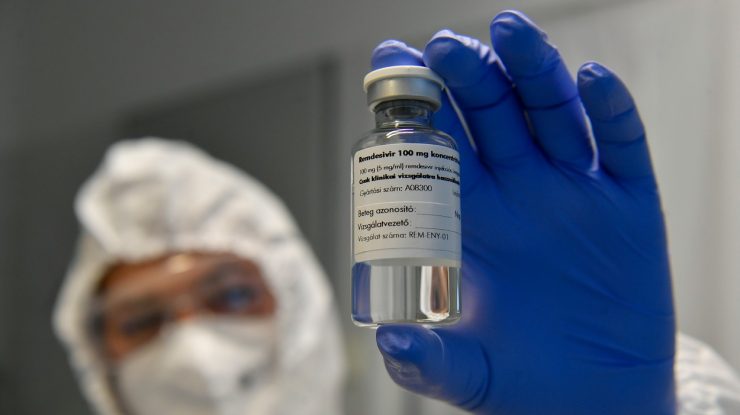
- Uniunea Europeană a aprobat condiționat Remdesivir, primul tratament anti-Covid de pe continent, în iulie 2020.
- La începutul acestei luni, producătorul american Gilead a prognozat vânzări în 2021 de până la 3 miliarde de dolari pentru Remdesivir.
- Pe 20 noiembrie OMS spunea că nu recomanda acest antiviral, deoarece nu exista nimic care să sugereze un „efect semnificativ asupra mortalității.
Autoritatea europeană de reglementare a medicamentelor a declarat marți că se așteaptă să-și dea avizul înainte de vară dacă Remdesivirul de la Gilead Sciences poate fi utilizat pentru a trata pacienții cu COVID-19 care nu au nevoie de oxigen, transmite Reuters.
Indicația pentru utilizarea prelungită, dacă este aprobată, ar oferi terapie antivirală mai multor pacienți, pe măsură ce infecțiile cu coronavirus cresc și sistemele de asistență medicală sunt supuse presiunii din cauza variantelor de virus emergente și extrem de transmisibile.
Dezvoltatorul american Gilead a trimis date Agenției Europene pentru Medicamente (EMA), a declarat observatorul, adăugând că Comitetul său pentru medicamente de uz uman a început să evalueze cele mai recente comunicări.
Uniunea Europeană a aprobat condiționat Remdesivir, primul tratament COVID-19 de pe continent, în iulie anul trecut pentru tratamentul COVID-19 la adulți și adolescenți cu vârsta peste 12 ani cu pneumonie care necesită tratament.
Orice potențială aprobare din partea EMA, care trebuie aprobată în mod oficial de Comisia Europeană, ar ajuta, de asemenea, Gilead să extindă vânzările unui tratament care a contribuit la creșterea vânzărilor sale din al patrulea trimestru.
La începutul acestei luni, producătorul american de medicamente a prognozat vânzări în 2021 de până la 3 miliarde de dolari pentru Remdesivir, vândute sub marca Veklury.
Pe 8 octombrie, Comisia de la Bruxelles a semnat un acord cu firma Gilead pentru a permite statelor europene să cumpere 500.000 de doze de Remdesivir. La aproximativ 2.000 de dolari pe doză intravenoasă, aceasta trebuia să aduca Gilead un beneficiu până la 1.035 miliarde de dolari. O sumă care s-ar fi adăugat la cele 900 de milioane de dolari pe care medicamentul le-a adus deja în laboratorul american în al treilea trimestru al anului 2020.
Dar pe 20 noiembrie Organizația Mondială a Sănătății a anunțat însă că nu recomanda acest antiviral, deoarece nu exista nimic care să sugereze un „efect semnificativ asupra mortalității, utilizarea ventilației mecanice, accelerarea„ îmbunătățirii stării clinice și a altor stări de sănătate importante rezultatele pacientului ‘. Oamenii de știință care au efectuat cele patru studii clinice pe care s-a bazat OMS, au ridicat chiar „posibilitatea unor efecte secundare semnificative”.
Studiul clinic european Discovery a retras, de asemenea, Remdesivir din studiul său din 27 ianuarie, „din lipsă de dovezi ale eficienței sale”.
Punctul culminant al scandalului a fost că Comisia Europeană, care va trebui să aprobe unda verde de la EMA, a fost totuși deturnată de Gilead în octombrie. Când a fost semnat acordul, laboratorul american aflase de rezultatele negative ale studiului Solidarity … spre deosebire de Comisia Europeană, care nu a fost informată decât a doua zi